Профессор ЛУ Мин: Новые достижения в разработке препаратов для лечения нейроэндокринных опухолей
2025-4-15Несмотря на стремительный прогресс в разработке новых противоопухолевых лекарственных препаратов во всём мире, в центре внимания исследователей находят в основном наиболее распространённых типы рака, таких как рак лёгкого, желудка и колоректальный рак. На редко встречающиеся нейроэндокринные опухоли (НЭО) относительно редко обращает внимание научное сообщество. Однако, к счастью, китайские специалисты по данному направлению активно продвигают развитие этого направления, благодаря чему некоторые препараты НЭО уже начали применяться в клинических испытаниях.
В данной статье ЛУ Мин, главный врач отделения гастроинтестинальной онкологии Пекинской онкологической больницы/Пекинской больницы GoBroad, поделится впечатляющими достижениями в области разработки новых препаратов для лечения нейроэндокринных опухолей за 2025 года, раскрывая новейшие тенденции в лечении НЭО и вселяя новые надежды для пациентов.
Ⅰ. Текущая ситуация лечения нейроэндокринных опухолей
1. Нейроэндокринные опухоли (NET)
Для нейроэндокринных опухолей ЖКТ и поджелудочной железы (PanNET) имеется несколько вариантов лечения, включая октреотид, ланреотид, эверолимус и сунитиниб. Кроме того, важную роль играют такие препараты и методы, как суруфатиниб, капецитабин, темозоломид и пептидная рецепторная радионуклидная терапия (PRRT). Однако для нейроэндокринных опухолей лёгкого (LungNET) доступно значительно меньше лекарственных препаратов.
2.Нейроэндокринный рак (NEC)
Варианты методов лечения при нейроэндокринном ракае (NEC) ещё более ограничены. Согласно рекомендациям CACA, для NEC рекомендуется комбинированная химиотерапия на основе платины. Схемы первой линии включают этопозид + цисплатин (EP), этопозид + карбоплатин (EC) и иринотекан + цисплатин (IP)
II. Новые достижения в лекарственной терапии нейроэндокринных опухолей
- Иммунотерапия
Иммунотерапия стала одним из основных методов лечения многих видов злокачественных опухолей, однако её применение при нейроэндокринных новообразованиях имеет сложную специфику. Нейроэндокринные опухоли подразделяются на высокодифференцированные нейроэндокринные опухоли (NET) и низкодифференцированные нейроэндокринные карциномы (NEC). Для обеих категорий иммунотерапия не является рекомендуемым методом лечения. Это объясняется тем, что эффективность моноиммунотерапии обычно не превышает 5%, а даже при комбинации двух иммунопрепаратов (двойная иммунотерапия) показатель эффективности составляет лишь около 10%.
Тем не менее, в определённых ситуациях в клинике иммунотерапия может быть полезной для пациентов с нейроэндокринными опухолями. Например, у некоторых пациентов с высокодифференцированными нейроэндокринными опухолями поджелудочной железы после применения моноиммунотерапии наблюдалась значительная регрессия опухоли. Также бывают случаи, когда опухоль была контролирована только при монотерапии в течение более двух лет. Однако ключевым вызовом в клинической практике остаётся идентификация таких пациентов: в настоящее время на основе данных предыдущих клинических исследований мы разрабатываем новый тест для иммуногистохимического определения PD-L1 с целью более точного отбора целевой группы пациентов.
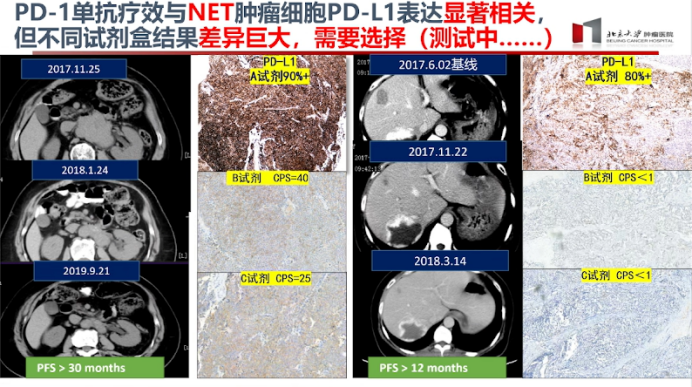
Что касается нейроэндокринных опухолей внелегочного происхождения, хотя некоторые препараты иммунотерапии (такие как ниволумаб и пембролизумаб) уже одобрены к применению, но из-за низкой эффективности монотерапии исследователи активно изучают различные комбинированные схемы лечения. Несмотря на эффект комбинированной иммунотерапии при мелкоклеточном раке легкого, для нейроэндокринных опухолей внелегочной происхождения пока отсутствуют данные масштабных исследований III фазы, которые могли бы поддержать её эффективность как стандартного лечения. Поэтому иммунотерапия пока не получила широкого применения в лечении нейроэндокринных опухолей.
- Таргетный препарат: LBL-024 (PD-L1/4-1BB)
LBL-024 представляет собой биспецифическое антитело, которое блокирует иммуносупрессивный путь опухолевых клеток через таргетинг PD-L1, одновременно эффективно локализуя костимулятор 4-1BB в опухолевом микроокружении для усиления противоопухолевого иммунного ответа. В монотерапии нейроэндокринных опухолей внелегочного происхождения LBL-024 продемонстрировал показатель объективного ответа (ORR) в 33,3% случаев и уровень контроля заболевания (DCR) в 51,1% случаев, что значительно превышает показатели существующих схем терапии второй линии. Этот препарат получил статус орфанного лекарственного средства от Управления по контролю за пищевыми продуктами и лекарственными препаратами США (FDA), и в настоящее время проводятся регистрационные испытания, а также клинические исследования комбинации с EP в первой линии терапии.
3. Препараты, нацеленные на DLL3
Мишень DLL3 представляет собой актуальный предмет исследования лечения нейроэндокринных опухолей в последние годы. Она экспрессируется примерно в 80% случаев мелкоклеточного рака лёгкого и других нейроэндокринных опухолей, при этом практически отсутствует в нормальных тканях. В настоящее время ведётся активная разработка препаратов, нацеленных на DLL3, включая BI 764532, HPN 328 и тарлатумаб, которые в клинических испытаниях продемонстрировали высокую эффективность и уровень контроля заболевания.
- HPN 328 — разрабатываемый за рубежом препарат, который помимо связывания с CD3 ещё содержит в себе антиальбуминовый компонент, увеличивающий его период полувыведения. В группе эффективной дозы при мелкоклеточном раке лёгкого HPN 328 демонстрирует 39% объективного ответа, а при других опухолях - до 46%.
- Тарлатумаб (Tarlatamab) представляет собой биспецифическое T-клеточное антитело (BiTE), нацеленное на DLL3 и CD3. В исследованиях I фазы при мелкоклеточном раке лёгкого показатель объективного ответа препарата составил 23,4%, уровень контроля заболевания — 51%. В исследованиях II фазы оптимальной была признана дозовая группа 10 мг, которая продемонстрировала эффективность выше 30%. 16 мая 2024 года FDA одобрило тарлатумаб для лечения распространённого мелкоклеточного рака лёгкого после прогрессирования на платиновой химиотерапии. Наиболее частыми нежелательными явлениями являются цитокиновый шторм и нейротоксичность, которые можно контролировать симптоматической терапией.
- BI 764532 — это IgG-подобное биспецифическое антитело, связывающее T-клетки. Данный препарат хорошо зарекомендовал себя в лечении DLL3-позитивного мелкоклеточного рака лёгкого и нейроэндокринных опухолей. В клинических испытаниях общее число участников с мелкоклеточным раком лёгкого составило 150 пациентов, тогда как в группе нейроэндокринных опухолях внелёгочного происхождения было включено 66 пациентов. В группе внелегочных нейроэндокринных опухолей BI 764532 показал объективный ответ (ORR) в 26% случаев и уровень контроля заболевания (DCR) в 45%. Результаты впечатляют.
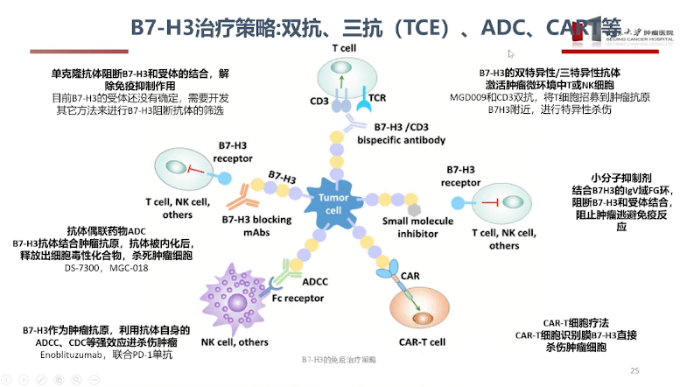
4. Препараты, нацеленные на B7-H3
Мишень B7-H3 привлекает внимание экспертов по иммунотерапии благодаря своей экспрессии при различных типах рака, особенно при мелкоклеточном раке лёгкого (МРЛ). В настоящее время разработка препаратов, направленных на B7-H3, продвигается быстрыми темпами. В препараты включаются биспецифические антитела, триспецифические антитела (TCE), конъюгированные с антителами лекарственные средства (ADC) и CAR-T-клетки.
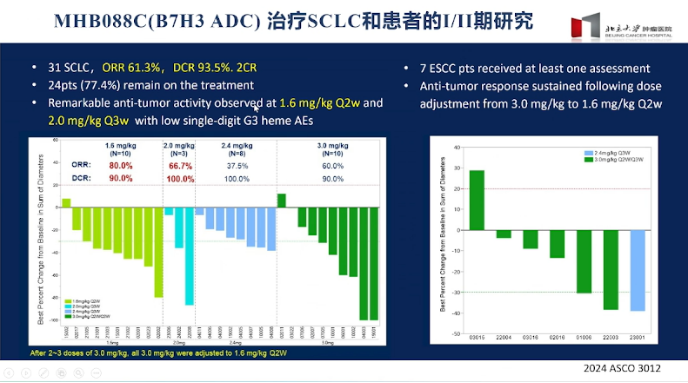
- DS-7300 представляет собой конъюгаты «антитело-лекарственное средство» (ADC), содержащие лекарство химиотерапии сmptothecin. В клинических испытаниях DS-7300 продемонстрировал объективный ответ (ОР) в 52,4% случаев среди 22 пациентов с мелкоклеточным раком лёгкого, медиану общей выживаемости (ОВ) — 12,2 месяца и медиану выживаемости без прогрессирования (ВБП) — 5,6 месяца.
- MHB088C представляет собой препарат китайской разработки, который уже прошёл клинические испытания и продемонстрировал при лечении мелкоклеточного рака лёгкого объективный ответ в 61,3% случаев и уровень контроля заболевания на уровне 93,5%, что превосходит показатели DS-7300.
5.Препараты, нацеленные на SEZ6
SEZ6 — трансмембранный белок, экспрессирующийся при мелкоклеточном раке лёгкого, нейроэндокринных опухолях и опухолях центральной нервной системы(ЦНС).
- ABBV-706 — новый препарат, нацеленный на SEZ6, который в настоящее время проходит клинические исследования I-II фазы за рубежом. Препарат продемонстрировал большой потенциал в лечении мелкоклеточного рака лёгкого с объективным ответом в 43,8%, внелегочных нейроэндокринных опухолях — эффективность составила 28%. Несмотря на то, что на сегодня исследование ABBV-706 пока находится на ранней стадии, препарат показывает впечатляющие результаты при определённых типах злокачественных опухолей. Уникальный механизм действия и впечатляющие показатели эффективности позволяют предположить, что данный препарат станет объектом исследований как международных, так китайских фармацевтических компаний в ближайшем будущем.
6. Препараты, нацеленные на Trop2 и Claudin 18.2
- Trop2 (полное название - антиген поверхности клеток трофобласта 2) представляет собой трансмембранный белок, который значительно экспрессируется при различных типах злокачественных опухолей. Данные по экспрессии в нейроэндокринных опухолях показывают: высокий уровень экспрессии при нейроэндокринных карциномах (NEC) - 37,1%, высокий уровень экспрессии при нейроэндокринных опухолях (NET) - 15,3%. В поджелудочной железе и желудке показатели составляют 50% и 40% соответственно. В связи с широкой экспрессией Trop2 в опухолях, учёные активно ведут разработки препаратов против этой мишени. Уже зарегистрированы ADC-препараты, нацеленные на Trop2, которые предоставляют новые терапевтические возможности для пациентов с опухолями, характеризующимися высокой экспрессией этого маркера. При отсутствии других оптимальных вариантов лечения, Trop2-ADC препараты могут рассматриваться как потенциальный метод лечения.
- Claudin 18.2 — белок плотных контактов, экспрессия которого была хорошо изучена при раке желудка и поджелудочной железы. Хотя его экспрессия при нейроэндокринных опухолях пока не изучена в полной мере, имеющиеся данные свидетельствуют, что значительная часть пациентов с нейроэндокринными опухолей желудочного и панкреатического происхождения экспрессируют Claudin 18.2.
III. Заключение
По мере появления новых препаратов и методов лечения перспективы лечения нейроэндокринных опухолей (НЭО) становятся все более обнадеживающими. Мы с нетерпением ждём завершения клинических испытаний этих новых лекарственных средств, которые смогут предоставить пациентам более эффективные варианты лечения. Мы также будем продолжать следить за прогрессом в исследованиях этих препаратов и прилагаем все усилия для внедрения их в клиническую практику лечения нейроэндокринных опухолей.






